Врачи Европейского медицинского центра Абдуллин Искандер и Баранова Екатерина рассказывают о прицельной биопсии и ее роли в выявлении рака предстательной железы
Два, казалось бы, одинаковых пациента потребовали абсолютно различных подходов в лечении. Отличить злокачественную опухоль позволила прицельная биопсия. О роли fusion-биопсии (Подробнее о Фьюжн-биопсии) и консенсусе, опубликованном в январе текущего года, – на примере собственной клинической практики.
Когда негативную биопсию действительно можно считать негативной? Поднимая этот вопрос, Stacy Loeb в январской публикации Journal of Urology 2017 г. отмечает, что традиционная рандомная биопсия не позволяет быть уверенным в негативности негативного ответа. По данным SEER (Surveillance, Epidemiology, and End Results), почти 12% пациентов с негативной биопсией в течение года потребовалось проведение повторной биопсии; почти 40% — повторить процедуру пришлось в течение 5 лет. Более того, даже полученный положительный результат биопсии достаточно часто недооценен. Так, более чем у трети пациентов с раком предстательной железы (РПЖ) низкого или очень низкого риска при проведении повторной биопсии или простатэктомии в течение 6 мес оценка по шкале Глисона была увеличена.
И если еще пару лет назад ученые ставили вопрос о том, какими же методами все-таки дифференцировать пациентов для лечения и активного наблюдения, то в 2017 г. они пришли к консенсусу: AUA и SAR рекомендуют для пациентов с первой негативной биопсией, но растущим или высоким уровнем простатического специфического антигена (ПСА), выполнять мульти-параметрическая магнитно-резонансная томография (мпМРТ), если PI-RADS находится в пределах от 3 до 5, пациентам показана повторная прицельная fusion-биопсия.
Одинаковые пациенты
В урологической клинике ЕМС (Центр Онкоурологии) введен и выполняется метод fusion-биопсии предстательной железы (ПЖ). Наш опыт недостаточен для проведения статистических исследований, однако предлагаемые клинические примеры наглядно демонстрируют эффективность и необходимость ее внедрения в клиническую практику.
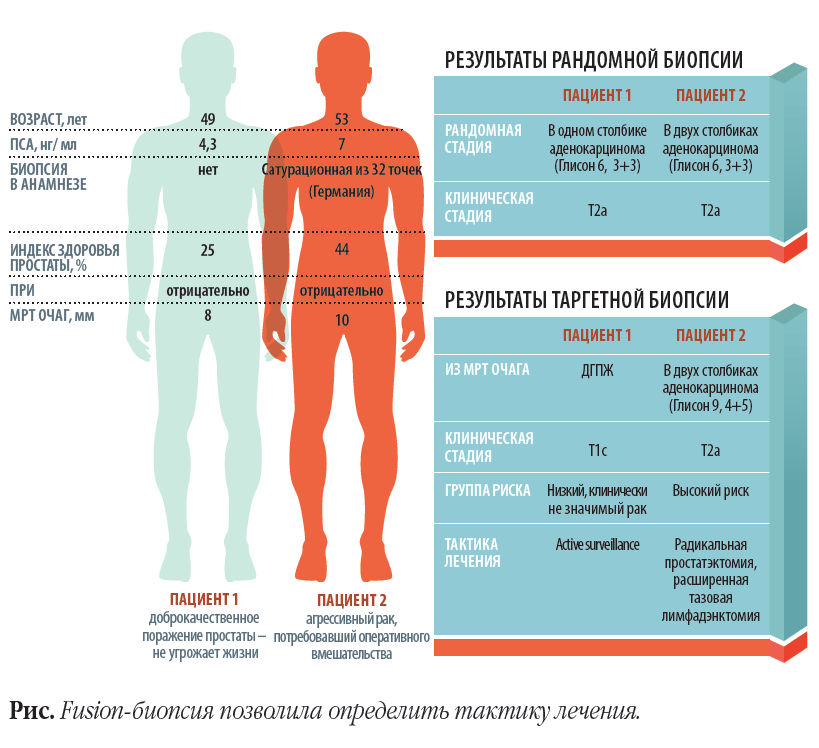
Итак, в урологической клинике ЕМС обследование прошли 2 пациента, сопоставимых по возрасту, уровню общего ПСА, индексу здоровья ПЖ (Phi), а также выявленному при МРТ диаметру матологического очага. Один из пациентов, у которого впоследствии был выявлен РПЖ (Глисон 9, 4+5), ранее перенес сатурационную биопсию ПЖ из 32 точек с отрицательным результатом. Обоим пациентам выполнена рандомная и таргетная биопсии. По результатам 1-й биопсии оба пациента имеют аденокарциному со степенью злокачественности по шкале Глисон 6 (3 + 3) и распределены в группу низкого риска РПЖ.
Однако при выполнении таргетной биопсии из подозрительных очагов, по данным мпМРТ, пациентам поставлены различные диагнозы: одному — доброкачественная гиперплазия ПЖ (ДГПЖ), а другому — аденокарцинома со степенью злокачественности по Глисону 9 ( 4+5).
Таким образом, выполнение мпМРТ и прицельной биопсии существенно изменило не только оценку гистологической природы опухоли, но также дифференцировала тяжелый случай рака от неактивного, клинически не значимого, что полностью изменило тактику лечения и ведения пациентов.
Биопсия: вехи и прорехи
Пациентам с РПЖ среднего и высокого риска радикальная терапия улучшает показатели выживаемости. Поэтому точное диагностирование РПЖ и определе-ние степени риска имеет решающее значение в выборе лечебной тактики. Ошибочное определение степени риска РПЖ может привести как к избыточно-му лечению, так и к недостаточному, в том числе к упущению так называемого «окна излечимости».
Постепенный переход к рекомендациям о повышении числа биопсийных точек более 12 не позволили существенно улучшить чувствительность метода, высший уровень которого достигает 30%. В прошлом основной локализацией РПЖ в 85% случаев считалась периферическая зона кзади от мочеиспускательного канала, и только 15% случаев обнаружено в передней области. Отмеченные данные, вероятно, не представляют истинную распространенность заболевания в различных анатомических областях ПЖ, а результат основан на случайных биопсиях под контролем трансректального ультразвукового исследования (ТРУЗИ) ПЖ.
Начиная с 2000-х гг. для повышения как чувствительности метода, так и рентабельности биоптатов ПЖ выбраны и изучены 2 основных подхода:
- улучшение качества биопсийного материала путем увеличения числа биопсий и их распределение в частях ПЖ: сатурационная биопсия; трансперинеальная биопсия через решетку;
- повышение адресности биопсии в стремлении установить потенциальные раковые области.
В настоящее время все усилия направлены на улучшение точности диагностики при РПЖ для обеспечения большей уверенности, с которой врач и пациент будут принимать решение о вариантах лечения.
На современном этапе мпМРТ уже широко применяется в урологии, и ее включение в стандартный набор методик у пациентов с подозрением на РПЖ — объективная необходимость. Магнитно-резонансная томография (МРТ) признается прямым и неинвазивным методом для предварительной оценки наличия РПЖ. Сочетание анатомических изображений (высокое разрешение T2-взвешенных изображений) с функциональными методами визуализации, включая диффузионно-взвешенные изображения (ДВИ), динамически контрастированную томографию (DCE) и МР-спектроскопию (то есть мпМРТ), значительно улучшает точность диагностики РПЖ, позволяя обнаруживать опухоль и ее локализацию. Многие исследователи сообщили, что у пациентов с повышенным уровнем ПСА и отрицательными систематическими биопсиями под ТРУЗИ-наведением — исследование МРТ повышает обнаружение РПЖ от 21 до 52%.
Техника выполнения таргетной биопсии заключается в использовании сенсора положения, прикрепленного к датчику, что позволяет импортиро-вать объемные данные в формате DICOM разных модальностей, в нашем случае с мпМРТ ПЖ и совмещать с полученными ультразвуковыми изображениями. В результате врач видит ультразвуковое изображение в реальном времени одновременно с соответствующим срезом изображе-ния, полученным на мпМРТ. Далее любое изменение положения ультразвукового датчика автоматически изменит картинку среза объемного изображения. Выполнение прицельной биопсии состоит из нескольких этапов.
Этап №1 — подготовка. Для работы с объемной навигацией требуется рядом с ультразвуковым аппаратом создать магнитное поле. Для этого излучатель магнитного поля располагается на стойке непосредственно рядом с кушеткой. Далее при помощи специальной скобы магнитные сенсоры (приемники) крепятся на ультразвуковой датчик. Эти сенсоры определяют положение датчика в пространстве относительно пациента. Излучатель и оба приемника подключаются к передней панели ультразву-ковой системы.
Этап №2 — импорт изображений. Требуется загрузить трехмерный объем данных. Эти данные могут быть получены на МРТ, а также при 3D/4D УЗИ. Главное условие — формат DICOM. Импорт возможен как по сети, так и с внешнего носителя (CD/DVD, USB). После активации опции и загрузки 3D-снимков на экране появится похожее изображение.
Этап №3 — работа с изображениями. Теперь необходимо справа выбрать томографический срез и получить слева такой же срез ультразвуковым датчиком. После этого изображения помечаются как эквивалентные. Дальше любое изменение положения ультразвукового датчика автомати-чески изменит правую картинку среза объемного изображения.
Достаточное количество серийных исследований указывают на важность использования МРТ/ультразвукового слияния при выполнении fusion-биопсии для активного наблюдения пациентов с РПЖ низкого риска. Уолтон Диас и др. сообщили о небольшой когорте пациентов, перенесших вначале систематические биопсии, а в последующем fusion-биопсию. Прицельная повторная биопсия привела к пересмотру гистологической шкалы Глисона и снижению степени злокачественности (GS менее 7) у 22% пациентов на основе только МРТ-ультразвукового слияния.
Кроме того, Delongchamps и его коллеги продемонстрировали обнаружение рака в группе пациентов, имеющих fusion-биопсию, по сравнению с систематической 12-точечной ТРУЗИ-биопсией (76% против 33% пациентов, р = 0,0016). Результаты Рудь и других также подчеркивают, что более высокое подозрение МРТ поражения имеют большую склонность содержать РПЖ в прицельных биоптатах.
Теперь не только по данным литературы, но и по собственному опыту мы можем говорить о том, что fusion-биопсии ПЖ позволяют существенно повысить выявляемость клинически значимых форм РПЖ и использование fu-sion-биопсии в клинической практике будет способствовать выработке оптимальной и индивидуальной тактики лечения пациентов с РПЖ.
Журнал "Урология сегодня" №1 (46) 2017
ПОЛЕЗНЫЕ ССЫЛКИ

Вопросы и ответы
Отзывы
| Осмотр врачом-психиатром с выездом на дом за пределы МКАД до 30 км | 733 у.е. / 72 502 руб. |
| Выезд врача-специалиста на дом в пределах МКАД | 358 у.е. / 35 410 руб. |
| Выезд врача-специалиста на дом за пределы МКАД до 10 км | 424 у.е. / 41 939 руб. |
| Выезд врача-специалиста на дом за пределы МКАД до 30 км | 535 у.е. / 52 918 руб. |
| Выезд врача-специалиста на дом за пределы МКАД до 50 км | 656 у.е. / 64 886 руб. |
Специалисты
Контакты




